La prochaine révolution en biologie ne consiste pas à lire le code de la vie, mais à l’écrire. (…) L’écriture de l’ADN est encore plus prometteuse, car elle offre la possibilité de guérir n’importe quelle maladie. Andrew Hesel. 23 octobre 2025. Source.
Thème du mois : Les mitochondries
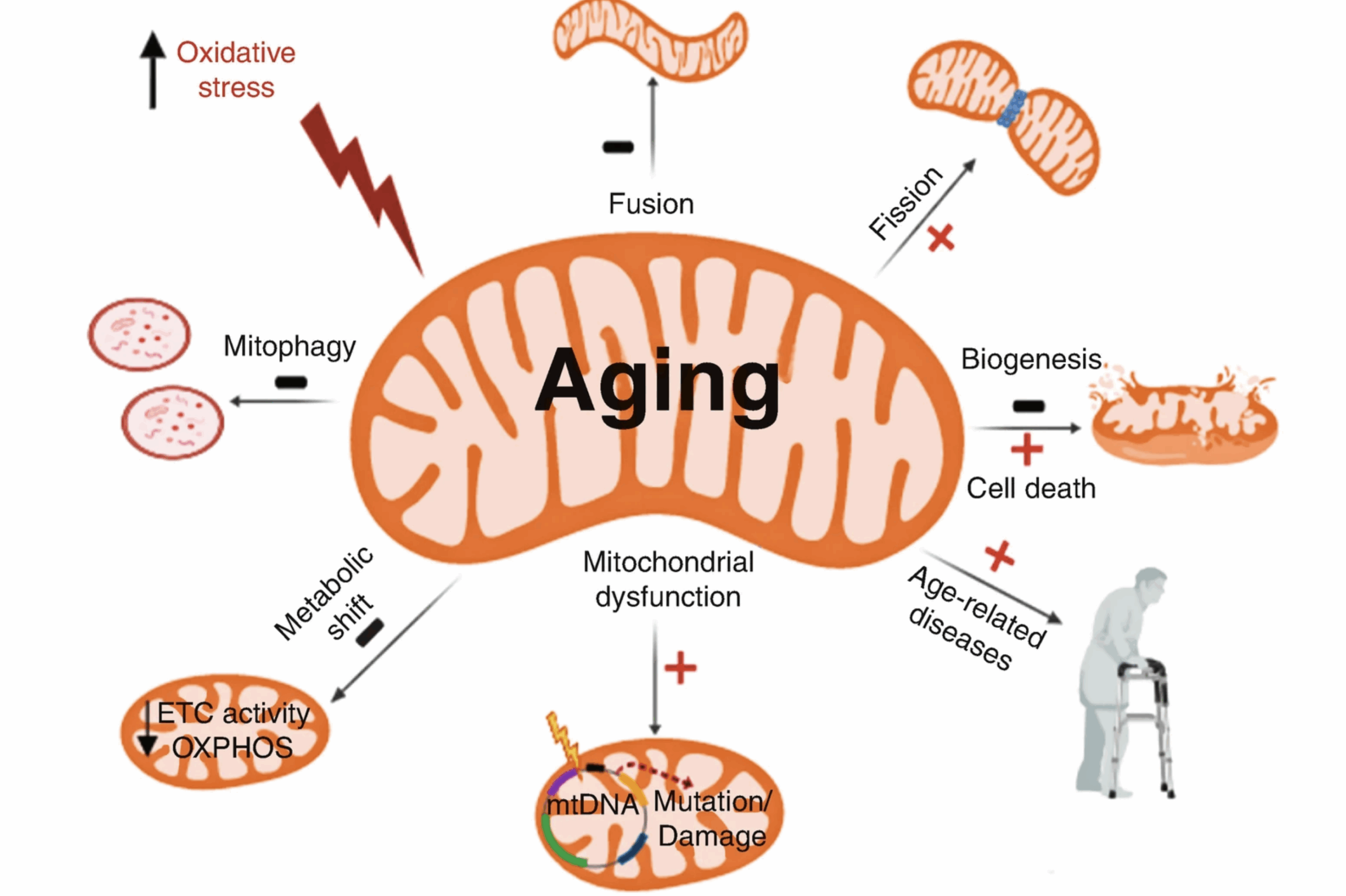
La centrale énergétique et l’horloge : comment les mitochondries influencent le vieillissement
Il y a environ 2,3 milliards d’années, un organisme a absorbé une bactérie qui allait devenir une mitochondrie. Pour les animaux, il s’agissait de la symbiose la plus réussie de l’histoire de la vie. Aujourd’hui, les mitochondries, souvent appelées les « centrales énergétiques » de la cellule, font bien plus que simplement produire de l’énergie. Ces organites petits mais puissants génèrent de l’ATP, la molécule essentielle qui alimente presque tous les processus cellulaires, tout en régulant l’équilibre calcique, l’apoptose (mort cellulaire programmée) et les voies métaboliques clés. Ce qui les rend particulièrement intrigantes, c’est qu’elles contiennent leur propre ADN, distinct du noyau cellulaire, ce qui les rend particulièrement vulnérables aux dommages au fil du temps.
Les mitochondries subissent une usure qui affecte leur capacité à fonctionner correctement.
1. ADN endommagé, cellules endommagées
Les mitochondries possèdent leur propre ADN (ADNmt), distinct de l’ADN nucléaire de la cellule. Contrairement à l’ADN nucléaire, l’ADNmt ne dispose pas des histones protectrices robustes et des systèmes de réparation qui le protègent contre les dommages. Cela le rend particulièrement vulnérable au stress oxydatif, c’est-à-dire au bombardement constant de molécules réactives produites lors de la production d’énergie. Au fil du temps, le stress oxydatif introduit des mutations dans l’ADNmt, perturbant les gènes responsables des composants clés de la chaîne de transport des électrons.
- Le paradoxe des ROS
Les espèces réactives de l’oxygène (ERO) sont une arme à double tranchant en biologie. D’une part, elles sont des sous-produits naturels de la respiration mitochondriale et jouent un rôle important dans la signalisation pour l’adaptation, la réparation et la défense immunitaire des cellules. Dans les cellules jeunes et saines, de faibles niveaux d’ERO agissent comme des messagers bénéfiques qui ajustent le métabolisme et déclenchent des réponses antioxydantes protectrices, un processus connu sous le nom de mitohormèse. Cependant, à mesure que les mitochondries vieillissent et deviennent moins efficaces, elles produisent des ROS en excès qui submergent les défenses antioxydantes de la cellule. Cette surcharge oxydative endommage l’ADN, les lipides et les protéines, altérant les structures cellulaires et les voies de signalisation. Au fil du temps, ces lésions moléculaires s’accumulent, accélérant la dégénérescence des tissus et contribuant à des maladies telles que la maladie d’Alzheimer, la maladie de Parkinson et le déclin cardiovasculaire.
- Adieu l’ancien — ou pas
Les cellules disposent d’un système sophistiqué de contrôle de la qualité pour maintenir la santé mitochondriale, dont un élément central est la mitophagie, c’est-à-dire la dégradation et le recyclage ciblés des mitochondries endommagées. Dans des conditions normales, les mitochondries défectueuses sont marquées et éliminées pour faire place à de nouvelles mitochondries pleinement fonctionnelles. Cependant, avec l’âge, ce processus d’auto-renouvellement ralentit. Les mécanismes qui détectent et éliminent les mitochondries défectueuses deviennent moins réactifs, ce qui entraîne l’accumulation d’organites dysfonctionnels dans la cellule. Ces mitochondries défectueuses produisent non seulement moins d’énergie, mais libèrent également des molécules nocives qui exacerbent le stress oxydatif. L’accumulation progressive de mitochondries endommagées contribue de manière significative au déclin de la vitalité et de la résilience cellulaires observé dans les tissus vieillissants.
- Inflammation interne
Lorsque les mitochondries sont endommagées de manière irréversible, elles peuvent libérer des fragments de leur propre ADN et de leurs protéines dans le cytoplasme ou la circulation sanguine. Il est intéressant de noter que, comme l’ADN mitochondrial a évolué à partir d’anciennes bactéries, le système immunitaire le confond souvent avec un envahisseur étranger. Au fil du temps, cette inflammation persistante de faible intensité, appelée « inflammaging », devient un facteur majeur des lésions tissulaires liées à l’âge et des maladies chroniques, notamment l’athérosclérose, le diabète et la neurodégénérescence. Ainsi, les mitochondries défaillantes ne sont pas seulement victimes du vieillissement cellulaire, mais participent aussi activement à l’amplification des processus inflammatoires qui le sous-tendent.
Se concentrer sur les mitochondries pour lutter contre le vieillissement
Les progrès récents dans le domaine des mitochondries nano-conçues (systèmes biohybrides qui intègrent des mitochondries isolées à des nanomatériaux fonctionnels) pourraient bientôt nous permettre de les réparer et de les améliorer, ouvrant ainsi de nouvelles voies vers une meilleure santé et une plus grande longévité. Contrairement à la transplantation mitochondriale conventionnelle, qui consiste simplement à transférer des mitochondries saines vers des tissus endommagés, ces nano-biohybrides améliorent la stabilité des organites, stimulent la production d’ATP et permettent une administration ciblée. Les études précliniques montrent des résultats prometteurs dans les troubles cardiovasculaires, neurodégénératifs et liés à l’âge, notamment des percées où des mitochondries modifiées ont empêché la dégénérescence des disques intervertébraux chez les rats en restaurant la fonction mitochondriale et en modulant des voies de signalisation clés telles que mtDNA/SPARC-STING. En faisant le pont entre la science des matériaux et la biologie mitochondriale, les mitochondries nano-conçues pourraient devenir un nouvel outil puissant dans les thérapies de longévité, revitalisant le métabolisme énergétique à sa source.
Plusieurs stratégies sont en cours d’élaboration pour contrer le déclin mitochondrial. L’une des principales approches consiste à utiliser des antioxydants ciblant spécifiquement les mitochondries, tels que MitoQ et MitoVitE, qui visent à neutraliser l’excès de ROS et à réduire les dommages oxydatifs. Une autre approche se concentre sur la stimulation de la biogenèse mitochondriale, souvent par le biais de voies telles que l’activation de PGC-1α ; l’exercice physique reste la méthode la plus éprouvée à cet effet, mais des stimulants pharmacologiques sont à l’étude. Les thérapies qui améliorent la mitophagie, c’est-à-dire l’élimination sélective des mitochondries endommagées, suscitent également un intérêt croissant, car une mitophagie altérée est une caractéristique du vieillissement cellulaire. D’autres approches consistent à moduler le métabolisme mitochondrial, par exemple en augmentant les niveaux de NAD⁺, qui soutiennent les réactions redox mitochondriales et le métabolisme énergétique.
Parmi les thérapies expérimentales les plus prometteuses figure l’Elamipretide (SS-31), un peptide ciblant les mitochondries qui se lie à la cardiolipine dans la membrane mitochondriale interne, stabilisant sa structure et améliorant l’efficacité de la chaîne de transport des électrons. Dans les études précliniques, l’Elamipretide a amélioré l’endurance musculaire, la fonction cardiaque et l’énergie mitochondriale, et les premiers essais chez l’homme ont montré une augmentation de la production d’ATP chez les personnes âgées.
Collectivement, ces interventions ciblant les mitochondries représentent l’un des domaines les plus actifs de la recherche sur le vieillissement. Bien que la plupart d’entre elles en soient encore à un stade précoce de développement, elles illustrent une évolution thérapeutique plus large, passant du traitement de maladies liées à l’âge à la prise en charge des dysfonctionnements cellulaires sous-jacents qui sont à l’origine du vieillissement lui-même. Les interventions sur le mode de vie, telles que l’exercice physique et la modération calorique, restent les moyens les plus fiables pour préserver la santé mitochondriale, mais les essais en cours sur des peptides tels que l’Elamipretide, les précurseurs du NAD⁺ et les activateurs de la mitophagie pourraient bientôt élargir la panoplie d’outils permettant de promouvoir un vieillissement plus sain. Le succès de ce domaine dépendra de la capacité à surmonter des défis majeurs tels que la sécurité à long terme, la spécificité de l’administration et la démonstration d’améliorations réelles de la durée de vie en bonne santé chez l’homme, plutôt que de simples biomarqueurs cellulaires.
La bonne nouvelle du mois. Des cellules humaines réduisent les marqueurs de sénescence chez des macaques âgés.
Dans une étude publiée dans Cell (4 septembre 2025), des scientifiques ont démontré que l’injection de cellules progénitrices mésenchymateuses humaines résistantes à la sénescence (SRC) chez des macaques âgés réduisait considérablement les marqueurs du vieillissement et améliorait les fonctions cognitives, osseuses et reproductives.
C’est très prometteur. Il faut espérer que ces singes vivront assez longtemps pour démontrer que les cellules progénitrices prolongent la durée de vie en bonne santé.
Pour plus d’informations