Dépasser les limites connues de notre biologie pour prolonger la vie jusqu’à des extrêmes encore inatteignables est un rêve peut-être aussi vieux que l’humanité, mais nous disposons pour la première fois aujourd’hui d’outils adaptés pour le réaliser dans un proche futur. Les gènes et la longévité. Les défis de la science (publication du journal Le Monde). Page 11. 2018.
Thème du mois. Les limites de divisions cellulaires, cause ou effet du vieillissement ?
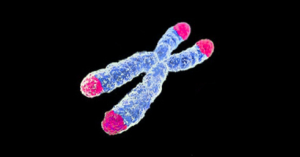 Aux extrémités de nos chromosomes, il y a une partie « non codante », n’ayant pas d’utilité directe connue, il s’agit des télomères. A chaque division cellulaire normale, une partie de ce télomère disparait. Lorsque le nombre de divisions a été important, l’ensemble de cette zone non codante a disparu et la cellule ne peut plus se diviser correctement. La limite du nombre de divisions (une cinquantaine pour une cellule humaine ordinaire) est appelée « limite de Hayflick« , du nom d’un biogérontologue qui découvrit ce mécanisme en 1965.
Aux extrémités de nos chromosomes, il y a une partie « non codante », n’ayant pas d’utilité directe connue, il s’agit des télomères. A chaque division cellulaire normale, une partie de ce télomère disparait. Lorsque le nombre de divisions a été important, l’ensemble de cette zone non codante a disparu et la cellule ne peut plus se diviser correctement. La limite du nombre de divisions (une cinquantaine pour une cellule humaine ordinaire) est appelée « limite de Hayflick« , du nom d’un biogérontologue qui découvrit ce mécanisme en 1965.
Cette limite ne concerne pas toutes les cellules. Les cellules-souches y échappent, mais aussi, malheureusement des cellules cancéreuses. Ainsi, les cellules d’Henrietta Lacks, décédée en 1951 d’un cancer foudroyant sont utilisées dans des milliers de laboratoires et se reproduisent toujours, presque 70 ans après sa mort, sans limitation.
Beaucoup ont vu dans la limite de division cellulaire la cause majeure du vieillissement. Lorsque les cellules ne peuvent plus se reproduire correctement, l’ensemble de l’organisme se dégrade petit à petit, inéluctablement. D’ailleurs, Leonard Hayflick lorsqu’il testa la limite des divisions cellulaires, s’était aperçu que les cellules des personnes plus âgées se divisaient moins souvent.
Des animaux qui ont des télomères qui se conservent plus longtemps ont une durée de vie plus longue (par exemple chez les chiens ou les oiseaux). De même, il y a une corrélation entre longueur de télomères et espérance de vie chez les humains.
Dans le cadre de cette explication du vieillissement, il y a une bonne nouvelle. La longueur des télomères peut être influencée de diverses manières. Ainsi, la télomérase est une enzyme qui, lors de la division cellulaire, permet le maintien de la longueur du chromosome en ajoutant une structure spécifique à chaque extrémité Certaines sociétés vendent des produits contenant de la télomérase, censé favoriser une vie plus longue.
La personne la plus célèbre parmi les expérimentateurs dans le domaine de la longévité, Liz Parrish a effectué en 2015 une thérapie génique. Le gène de la télomérase humaine (hTERT) qui régule à la hausse l’activité de l’enzyme télomérase a été injecté à plusieurs endroits pour faciliter sa dissémination dans tout le corps. Liz Parrish affirme que la longueur de ses télomères s’est considérablement allongée, ce qui établirait un rajeunissement biologique, pour cet aspect, de plus de vingt ans.
Malheureusement, les mécanismes du vieillissement sont un phénomène complexe. Un célèbre article scientifique intitulé « The Hallmarks of Aging » considère qu’il y a neuf causes principales du vieillissement. Aubrey de Grey de SENS en compte 7. Dans les deux théories, la question de la longueur des télomères ne concerne qu’une partie de ces causes. Il est donc très peu probable que l’allongement des télomères ait un effet fondamental en matière de longévité.
Mais même un effet positif qui ne ferait gagner « que » quelques années de vie est assez incertain. Il en va de la longueur des télomères comme de bien des aspects liés au vieillissement. Le sens de la causalité n’est pas certain. Ainsi, la décoloration des cheveux et les rides sont des conséquences et non des causes de la diminution des capacités dues à l’âge. Trouver un moyen de conserver la longueur des télomères pourrait donc être sans conséquence importante sur les autres aspects de la sénescence.
De plus, un des aspects principaux du vieillissement, c’est la dégradation neurologique (maladie d’Alzheimer notamment). Or, les neurones se divisent très peu ou pas.
Enfin, pour certain des partisans des théories des 7 ou 9 origines de la sénescence, ces causes forment un ensemble interdépendant et s’attaquer à l’une ou l’autre cause sans attaquer les autres sera sans réel effet. Un peu comme une voiture ne peut fonctionner si un seul élément ne fonctionne pas (une voiture ne roule pas sans essence, sans pneus, sans transmission,…), un corps humain ne peut fonctionner dans la durée que si une solution est trouvée pour toutes les causes.
Il est certain que beaucoup, voire tous les aspects de la sénescence, sont étroitement liés. Il est certain aussi que, pour ce qui concerne la durée de vie maximale, nous ne progressons plus ces dernières années malgré tous les progrès médicaux. Il est donc quasiment certain que les recherches à venir seront multidisciplinaires et complexes. Elles seront donc passionnantes d’un point de vue intellectuel et scientifique, outre leur immense utilité potentielle.
La bonne nouvelle du mois : encore un fonds pour la longévité
Un nouveau fonds pour investir dans les entreprises qui travaillent dans le domaine du vieillissement a récemment été lancé, le Longevity Vision Fund, un fonds de 100 millions de dollars. Selon Fight Aging, d’après ce qui a été dit et ce qui a été présenté à la conférence Longevity Leaders à Londres du 4 février 2019, il semble bien que les directeurs du Longevity Vision Fund souhaitent suivre les traces de Juvenescence, en se concentrant initialement sur la découverte de petites molécules pharmaceutiques.
Pour en savoir plus:
- De manière générale, voir notamment: heales.org, sens.org, longevityalliance.org et longecity.org
photo : un chromosome et ses télomères
