La vérité est, bien sûr, que la mort ne devrait pas plus être considérée comme un élément acceptable de la vie que la variole ou la polio, deux maladies que nous avons réussi à maîtriser sans nous dénoncer comme prétentieux. Alan Harrington, L’immortaliste. Source.
Le thème de ce mois-ci : Barrière hémato-encéphalique et vieillissement
Qu’est-ce que la barrière hémato-encéphalique (BHE) ?
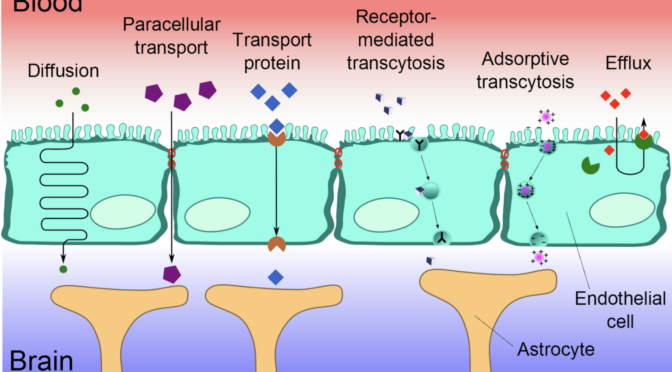
La BHE est une barrière hautement sélective formée par les cellules endothéliales des capillaires cérébraux, soutenues par des péricytes, des astrocytes et la matrice extracellulaire. Elle régule les échanges de substances entre la circulation sanguine et le cerveau, protégeant ce dernier des toxines, des agents pathogènes et des molécules inflammatoires, tout en laissant passer les nutriments et les gaz essentiels.
BHE et longévité
Avec l’âge, la BHE tend à devenir plus perméable, ce qui entraîne des problèmes de santé :
- Augmentation de la neuroinflammation : Les fuites de la BHE permettent aux cellules immunitaires périphériques et aux molécules inflammatoires de pénétrer dans le cerveau, contribuant ainsi à une neuroinflammation chronique.
- Accumulation de toxines : l’altération de la BHE entraîne une réduction de la clairance des substances neurotoxiques telles que la bêta-amyloïde, impliquée dans les maladies neurodégénératives telles que la maladie d’Alzheimer.
- Réduction du transport des nutriments : L’efficacité du transport des nutriments et de l’oxygène diminue, ce qui affecte la fonction neuronale et le métabolisme énergétique.
- Stress oxydatif : Les dommages oxydatifs liés au vieillissement compromettent davantage l’intégrité de la BHE, exacerbant le déclin cognitif.
Le processus de vieillissement a un impact significatif sur la barrière hémato-encéphalique (BHE), entraînant un déclin fonctionnel qui contribue aux maladies neurodégénératives et aux troubles cognitifs. La sénescence des cellules endothéliales associée à l’âge perturbe les jonctions serrées et augmente la perméabilité de la BHE, ce qui permet aux substances nocives de s’infiltrer dans le cerveau et d’en compromettre l’intégrité. Les cellules endothéliales cérébrales (CEB) sénescentes présentent également des altérations phénotypiques, notamment une altération de la régulation des jonctions serrées, ce qui aggrave le dysfonctionnement de la BHE au cours du vieillissement.
En outre, le déclin de la BHE varie selon les régions du cerveau et les facteurs démographiques, des études montrant un déclin plus marqué chez les hommes que chez les femmes dans les régions pariétales et temporales dès les années 60, probablement en raison de mécanismes de protection fondés sur le sexe. Les modifications structurelles des composants de la BHE, tels que les astrocytes et les péricytes, compromettent encore davantage son homéostasie, reliant ces altérations aux voies des maladies neurodégénératives. L’augmentation de la perméabilité de la BHE due à des facteurs de risque vasculaire tels que l’hypertension est également en corrélation directe avec les lésions de la substance blanche et le déclin cognitif, ce qui souligne l’importance de la santé vasculaire dans l’atténuation de ces effets.
Le maintien de l’intégrité de la BHE est essentiel pour la santé cognitive et la longévité globale :
- Réserve cognitive : La fonction intacte de la BHE favorise la santé neuronale, réduisant le risque de déclin cognitif lié à l’âge et de démence, déterminants majeurs de la qualité de vie chez les personnes âgées.
- Couplage neurovasculaire : Une fonction saine de la BHE favorise un couplage neurovasculaire optimal, essentiel à la plasticité cérébrale et aux mécanismes de réparation.
- Impact sur le vieillissement systémique : Le dysfonctionnement de la BHE peut entraîner une signalisation inflammatoire systémique, accélérant les processus de vieillissement dans d’autres systèmes organiques.
Plusieurs stratégies sont prometteuses pour maintenir l’intégrité de la BHE et favoriser la longévité :
L’exercice physique favorise la santé vasculaire, réduit l’inflammation et renforce l’intégrité de la BHE. Des études animales ont montré que l’exercice aérobie augmentait l’expression des protéines de la jonction serrée et réduisait le stress oxydatif. Le régime méditerranéen, riche en antioxydants, en acides gras oméga-3 et en polyphénols, réduit le stress oxydatif et l’inflammation, protégeant ainsi la BHE. Une restriction calorique modérée peut réduire la perméabilité de la BHE liée à l’âge en diminuant l’inflammation systémique. Les acides gras oméga-3 contenus dans l’huile de poisson renforcent l’intégrité de la BHE en réduisant l’inflammation et en favorisant la fonction des cellules endothéliales. Présents dans les baies, le thé vert et le chocolat noir, les flavonoïdes protègent contre le dysfonctionnement de la BHE grâce à leurs propriétés antioxydantes. Les vitamines E et C neutralisent les radicaux libres, protégeant ainsi les cellules endothéliales de la BHE des dommages oxydatifs.
L’axe cerveau-intestin et la barrière hémato-encéphalique (BHE)
Il s’agit de systèmes intimement liés qui jouent un rôle crucial dans le maintien de la santé neurologique et gastro-intestinale. L’axe cerveau-intestin est un réseau de communication bidirectionnel impliquant le système nerveux central, le système nerveux entérique, le microbiote intestinal et les systèmes immunitaire et endocrinien. Cet axe permet au cerveau et à l’intestin de s’influencer mutuellement par le biais de voies neuronales, hormonales, immunitaires et microbiennes. La BHE, quant à elle, sert de barrière protectrice qui régule le transport de substances entre la circulation sanguine et le cerveau. Le système nerveux central est ainsi protégé des toxines, des agents pathogènes et des fluctuations de la chimie du sang, tout en conservant l’accès aux nutriments et aux molécules de signalisation.
Les perturbations de la connexion cerveau-intestin-BHE ont des conséquences importantes sur la santé et la maladie. Des affections telles que les maladies neurodégénératives (par exemple, les maladies d’Alzheimer et de Parkinson), les troubles mentaux (par exemple, la dépression et l’anxiété) et les maladies auto-immunes (par exemple, la sclérose en plaques) sont de plus en plus souvent liées à un tel dysfonctionnement. De même, la dysbiose intestinale peut exacerber ces conditions en modifiant la production de neurotransmetteurs, les réponses immunitaires et la signalisation métabolique.
La BHE est constituée de cellules spécifiques. Pour protéger la barrière du vieillissement ou même la rajeunir, des traitements ciblant directement ces cellules peuvent être envisagés.
Sénolytiques : Une étude récente a examiné les biomarqueurs non invasifs et leurs réponses à une thérapie sénolytique combinant le dasatinib et la quercétine (D + Q) chez les souris PS19, un modèle de tauopathie largement utilisé. Cette étude a révélé que le traitement D + Q favorisait un changement du phénotype microglial d’un état associé à la maladie à un état homéostatique, réduisant les caractéristiques de la sénescence. En outre, les souris PS19 traitées au D+Q ont montré une amélioration des performances cognitives dans un test de conditionnement de la peur par traçage, ce qui indique une amélioration de la mémoire associée aux indices.
Inhibiteurs de mTOR : Les résultats d’une étude récente identifient l’activité de mTOR comme un facteur clé de la rupture de la BHE dans la maladie d’Alzheimer (MA) et potentiellement dans les troubles cognitifs d’origine vasculaire. Ils suggèrent également que la rapamycine et les composés apparentés (rapalogs) pourraient servir d’agents thérapeutiques pour restaurer l’intégrité de la BHE dans ces conditions. Cette étude met en évidence la cible mammalienne/mécanique de la rapamycine en tant que régulateur critique de la dégradation de la BHE dans les modèles de la maladie d’Alzheimer et des troubles cognitifs vasculaires. Elle souligne le potentiel des médicaments ciblant la mTOR pour restaurer l’intégrité de la BHE et atténuer la progression de la maladie.
Le polypeptide activateur de l’adénylate cyclase hypophysaire (PACAP) est une molécule naturelle qui a des effets protecteurs et de soutien de la croissance sur les cellules cérébrales. Comme le PACAP et son récepteur, le PAC1, sont présents dans les régions du cerveau touchées par la maladie d’Alzheimer, cette étude examine si le PACAP pourrait être un traitement utile de la maladie d’Alzheimer. Une étude a testé la PACAP sur un modèle murin de la maladie d’Alzheimer en administrant cette molécule quotidiennement par le nez aux souris pendant une période prolongée. Ce traitement a favorisé un traitement plus sain de la protéine précurseur de l’amyloïde (APP), ce qui a réduit la production de protéines bêta-amyloïdes (Aβ) nocives. Il a également augmenté les niveaux de facteur neurotrophique dérivé du cerveau (BDNF), qui favorise la santé cérébrale, et de Bcl-2, une protéine qui prévient la mort cellulaire.
Autres barrières du corps humain
1. Barrières physiques
Elles constituent la première ligne de défense pour bloquer l’entrée de substances ou d’organismes nocifs.
- La peau : Une couche externe résistante (stratum corneum) empêche l’entrée des agents pathogènes et minimise la perte d’eau. Elle agit comme un bouclier mécanique.
- Membranes muqueuses : Elles tapissent les cavités du corps (par exemple, les voies respiratoires, digestives et urogénitales). Produisent du mucus pour piéger les microbes et les particules.
- Les jonctions serrées : Elles se trouvent entre les cellules épithéliales de tissus tels que l’intestin et la barrière hémato-encéphalique, empêchant le passage de substances nocives.
2. Barrières chimiques
Il s’agit de substances produites par l’organisme pour neutraliser ou détruire les agents pathogènes.
- Niveaux de pH : L’environnement acide de l’estomac (acide gastrique, pH ~1,5-3,5) tue les agents pathogènes ingérés. Le pH de la peau et du vagin (légèrement acide) empêche la croissance microbienne.
- Enzymes : Les lysozymes présentes dans la salive, les larmes et le mucus décomposent les parois cellulaires bactériennes. Les enzymes digestives (par exemple, la pepsine dans l’estomac) dégradent les protéines microbiennes.
- Peptides antimicrobiens : Les défensines et les cathélicidines perturbent les membranes microbiennes et inhibent la croissance des agents pathogènes.
- Sueur et sébum : contiennent des composés antimicrobiens et créent un environnement inhospitalier pour les bactéries.
3. Barrières biologiques
Il s’agit d’organismes vivants ou de systèmes de l’organisme qui se protègent contre les agents pathogènes.
- Microbiote (flore) : Les bactéries commensales de l’intestin, de la peau et d’autres zones rivalisent avec les pathogènes pour les ressources et l’espace. Elles produisent des substances (par exemple, de l’acide lactique) qui inhibent les microbes nuisibles.
- Cellules immunitaires : Les phagocytes (par exemple, les macrophages, les neutrophiles) engloutissent et détruisent les agents pathogènes. Les cellules tueuses naturelles (NK) ciblent les cellules infectées ou anormales.
4. Barrières spécialisées
Certaines structures servent de mécanismes de protection avancés.
- Barrière placentaire : Protège le fœtus en régulant les échanges de nutriments, de gaz et de déchets tout en empêchant le passage de substances nocives.
- Barrière cornéenne : Elle protège l’œil et comprend une structure multicouche (épithélium, stroma et endothélium).
Toutes ces barrières, comme la BHE, perdent de leur efficacité avec l’âge. Cela se produit à des rythmes différents. Plus nous comprenons ce qui se passe, plus nous avons de chances de trouver de nouvelles thérapies. Et en 2025, nous avons encore beaucoup à découvrir sur la diversité des évolutions.
La bonne nouvelle du mois. Discussion ouverte sur l’édition (héréditaire) du génome.
Un article important sur la thérapie génique a été publié dans Nature : Nous devons parler de l’édition du génome humain. <<Dans quelques décennies, les technologies d’édition de gènes pourraient réduire la probabilité de maladies humaines courantes. Les sociétés doivent mettre à profit ce temps pour se préparer à leur arrivée. Les scientifiques connaissent des dizaines de milliers de variantes d’ADN associées à des maladies humaines. Prises isolément, la grande majorité de ces variantes ont des effets mineurs. Mais pris ensemble, les résultats peuvent être considérables>>.
Ce point de vue ouvre le débat sur d’éventuelles thérapies géniques pour les générations futures. Les maladies que nous pourrions guérir sont des maladies qui blessent et tuent principalement lorsque les gens vieillissent, puisque la mortalité des jeunes est aujourd’hui faible, particulièrement dans les pays les plus riches.
Pour plus d’informations