De volgende revolutie in de biologie is niet het lezen van de code van het leven, maar het schrijven ervan. (…) Het schrijven van DNA biedt nog grotere mogelijkheden: het potentieel om elke ziekte te genezen. Andrew Hesel. 23 oktober 2025. Bron.
Thema van deze maand: Mitochondriën
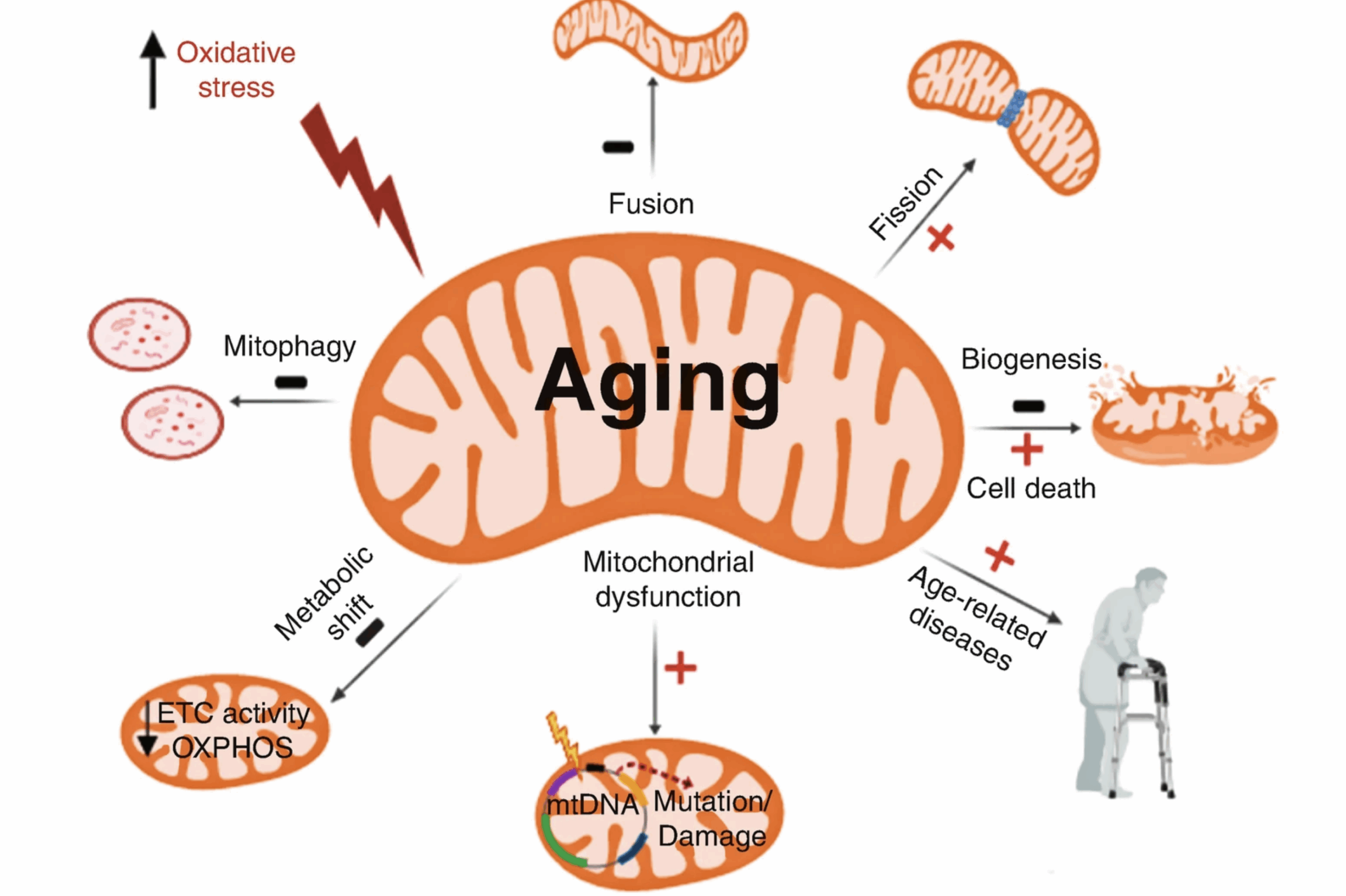
De krachtcentrale en de klok: hoe mitochondriën veroudering beïnvloeden
Ongeveer 2,3 miljard jaar geleden nam een organisme een bacterie op die zou uitgroeien tot mitochondriën. Voor dieren was dit de meest succesvolle symbiose in de geschiedenis van het leven. Tegenwoordig doen mitochondriën, vaak de ‘krachtcentrales’ van de cel genoemd, veel meer dan alleen energie produceren. Deze kleine maar krachtige organellen genereren ATP, het essentiële molecuul dat bijna elk cellulair proces van brandstof voorziet, terwijl ze ook de calciumbalans, apoptose (geprogrammeerde celdood) en belangrijke metabolische routes reguleren. Wat ze bijzonder intrigerend maakt, is dat ze hun eigen DNA bevatten, los van de celkern, waardoor ze na verloop van tijd bijzonder kwetsbaar zijn voor schade.
Mitochondriën ondergaan slijtage die hun vermogen om goed te functioneren aantast.
1. Beschadigd DNA, beschadigde cellen
Mitochondriën hebben hun eigen DNA (mtDNA), los van het nucleaire DNA van de cel. In tegenstelling tot nucleair DNA mist mtDNA de robuuste beschermende histonen en reparatiesystemen die tegen schade beschermen. Dit maakt het bijzonder kwetsbaar voor oxidatieve stress – de constante bombardementen van reactieve moleculen die tijdens de energieopwekking worden geproduceerd. Na verloop van tijd veroorzaakt oxidatieve stress mutaties in mtDNA, waardoor de genen die verantwoordelijk zijn voor belangrijke componenten van de elektronentransportketen worden verstoord.
- De ROS-paradox
Reactieve zuurstofspecies (ROS) zijn een tweesnijdend zwaard in de biologie. Enerzijds zijn ze natuurlijke bijproducten van mitochondriale ademhaling en spelen ze een belangrijke rol bij de signaaloverdracht in celaanpassing, herstel en immuunafweer. In jonge, gezonde cellen fungeren lage niveaus van ROS als heilzame boodschappers die het metabolisme verfijnen en beschermende antioxidantreacties activeren – een proces dat bekend staat als mitohormese. Naarmate mitochondriën ouder worden en minder efficiënt worden, produceren ze echter overmatige ROS die de antioxidantafweer van de cel overweldigen. Deze oxidatieve overbelasting beschadigt DNA, lipiden en eiwitten, waardoor celstructuren en signaalwegen worden aangetast. Na verloop van tijd stapelen deze moleculaire beschadigingen zich op, waardoor weefseldegeneratie wordt versneld en ziekten zoals Alzheimer, Parkinson en cardiovasculaire achteruitgang worden bevorderd.
- Weg met het oude — of toch niet
Cellen hebben een geavanceerd kwaliteitscontrolesysteem om de gezondheid van de mitochondriën te behouden, en een centraal onderdeel van dit systeem is mitofage — de gerichte afbraak en recycling van beschadigde mitochondriën. Onder normale omstandigheden worden defecte mitochondriën gemarkeerd en verwijderd om plaats te maken voor nieuwe, volledig functionele mitochondriën. Met het ouder worden vertraagt dit zelfvernieuwingsproces echter. De mechanismen die defecte mitochondriën detecteren en verwijderen, reageren minder goed, wat leidt tot de ophoping van disfunctionele organellen in de cel. Deze beschadigde mitochondriën produceren niet alleen minder energie, maar lekken ook schadelijke moleculen die oxidatieve stress verergeren. De geleidelijke ophoping van beschadigde mitochondriën levert een belangrijke bijdrage aan de afname van de cellulaire vitaliteit en veerkracht die wordt waargenomen in verouderende weefsels.
- Ontsteking van binnenuit
Wanneer mitochondriën onherstelbaar beschadigd raken, kunnen ze fragmenten van hun eigen DNA en eiwitten afgeven aan het cytoplasma of de bloedbaan. Interessant is dat, omdat mitochondriaal DNA is geëvolueerd uit oude bacteriën, het immuunsysteem het vaak aanziet voor een vreemde indringer. Na verloop van tijd wordt deze aanhoudende, lichte ontsteking – inflammaging genoemd – een belangrijke oorzaak van leeftijdsgebonden weefselschade en chronische ziekten, waaronder atherosclerose, diabetes en neurodegeneratie. Op deze manier zijn defecte mitochondriën niet alleen het slachtoffer van cellulaire veroudering, maar ook actieve deelnemers die de onderliggende ontstekingsprocessen versterken.
Focus op mitochondriën voor anti-verouderingsinterventies
Recente ontwikkelingen op het gebied van nano-gemanipuleerde mitochondriën (biohybride systemen die geïsoleerde mitochondriën integreren met functionele nanomaterialen) kunnen ons binnenkort in staat stellen om ze te herstellen en te verbeteren, waardoor nieuwe wegen worden geopend naar een betere gezondheid en een langere levensduur. In tegenstelling tot conventionele mitochondriale transplantatie, waarbij simpelweg gezonde mitochondriën naar beschadigd weefsel worden overgebracht, verbeteren deze nano-biohybriden de stabiliteit van organellen, stimuleren ze de ATP-productie en maken ze gerichte afgifte mogelijk. Preklinische studies tonen veelbelovende resultaten bij cardiovasculaire, neurodegeneratieve en leeftijdsgebonden aandoeningen, waaronder doorbraken waarbij gemanipuleerde mitochondriën degeneratie van tussenwervelschijven bij ratten voorkwamen door de mitochondriale functie te herstellen en belangrijke signaalroutes zoals mtDNA/SPARC-STING te moduleren. Door een brug te slaan tussen materiaalkunde en mitochondriale biologie, kunnen nano-gemodificeerde mitochondriën een krachtig nieuw instrument worden in de levensverlengende geneeskunde, dat het energiemetabolisme bij de bron revitaliseert.
Er worden verschillende strategieën ontwikkeld om de achteruitgang van mitochondriën tegen te gaan. Een belangrijke aanpak betreft antioxidanten die specifiek op mitochondriën zijn gericht, zoals MitoQ en MitoVitE, die tot doel hebben overtollige ROS te neutraliseren en oxidatieve schade te verminderen. Een andere aanpak richt zich op het stimuleren van mitochondriale biogenese, vaak via routes zoals PGC-1α-activering; lichaamsbeweging blijft hiervoor de best gevalideerde methode, maar farmacologische versterkers worden momenteel onderzocht. Therapieën die mitofagie versterken – de selectieve opruiming van beschadigde mitochondriën – staan ook steeds meer in de belangstelling, aangezien een verminderde mitofagie een kenmerk is van verouderende cellen. Andere benaderingen zijn onder meer het moduleren van het mitochondriale metabolisme, bijvoorbeeld door het NAD⁺-gehalte te verhogen, wat de mitochondriale redoxreacties en het energiemetabolisme ondersteunt.
Een van de meest veelbelovende experimentele therapieën is Elamipretide (SS-31), een op mitochondriën gericht peptide dat zich bindt aan cardiolipine in het binnenste mitochondriale membraan, waardoor de structuur ervan wordt gestabiliseerd en de efficiëntie van de elektronentransportketen wordt verbeterd. In preklinische studies verbeterde Elamipretide het uithoudingsvermogen van de spieren, de hartfunctie en de mitochondriale energetica, en vroege studies bij mensen hebben een verhoogde ATP-productie bij oudere volwassenen aangetoond.
Samen vormen deze op mitochondriën gerichte interventies een van de meest actieve gebieden in het onderzoek naar veroudering. Hoewel de meeste zich nog in een vroeg stadium van ontwikkeling bevinden, illustreren ze een bredere therapeutische verschuiving: van de behandeling van afzonderlijke ouderdomsziekten naar het aanpakken van de onderliggende cellulaire disfuncties die veroudering zelf veroorzaken. Levensstijlinterventies zoals lichaamsbeweging en caloriebeperking blijven de meest betrouwbare manier om de gezondheid van mitochondriën te behouden, maar lopende proeven met peptiden zoals Elamipretide, NAD⁺-precursoren en mitofagie-activatoren zouden binnenkort het instrumentarium voor het bevorderen van gezonder ouder worden kunnen uitbreiden. Het succes van dit onderzoeksgebied zal afhangen van het overwinnen van belangrijke uitdagingen, zoals veiligheid op lange termijn, specificiteit van toediening en het aantonen van echte verbeteringen in de gezondheidsduur van mensen in plaats van alleen cellulaire biomarkers.
Het goede nieuws van de maand. Menselijke cellen verminderen senescentiemarkers bij oude makaken.
In een studie gepubliceerd in Cell (4 september 2025) toonden wetenschappers aan dat het toedienen van senescentie-resistente menselijke mesenchymale progenitorcellen (SRC’s) aan oude makaken de markers van veroudering aanzienlijk verminderde en de cognitieve, bot- en voortplantingsfuncties verbeterde.
Dit is veelbelovend. Het is te hopen dat deze apen lang genoeg zullen leven om aan te tonen dat de progenitorcellen de gezonde levensduur verlengen.
Voor meer informatie